Biochemical Reasons for the Presence of the Limiting Character of Thrheonine in Some Mammals and the Absence of the Limiting Character of Threonine in Humans
A6cmpaKMnBu- OHH H Te JKe He3aMeHbIe amHHOKcJIoTB MoYr 6bITb JHMTHpyIOOHMH DJIa ODHHX BNDOB KHBOTbIX H He 6bITb JHMTHpyIOOHMH DJIa DpyTHX PnP CXODHom paunHOe. TaK, TpeOHHH YBJIaETcJ JHMTHpyIOSeJ aHHOKcIOToJ pH NtOM JIN3HH YBJIaETcJ JHMTHpyIOSeJ aHHOKcIOToJ DJIa BCEX BNDOB KHBOTbIX. B cTaBe Ha 6hoXHMHueCKom ypOBHe IOKa3aHbI IIpHuHbHaJInyra JHMTHpyIOSeO xapaKtepa TpeOHHH Ha IIpHMepe CBHHn H YeIOBeka, a TakKe aHaJIN3HPUOTcJ IIpHuHb JHMTHpyIOSeO xapaKtepa ToH JIN HHOJ He3aMeHHMO aHHOKcIOToB, YTO IIpeCTabJIaET BaxHoCTb DJIa CoCTaBJeHHN paIHHOHOB.
## I. Oco6eHHocTHPipeBpaIeHnTpeOHnHa y MJIeKoIIHTaIOIIHX
Oco6eHHocmu Kama6oJU3Ma mpeOnHa y MleKoIumauux. Chapman K. [2] OTMeuaet, YTO y MJIeKOIIHTaHOIIHX HmeeTcra IBa IyTH KaTa6OJIIN3Ma TpeOHnHa: OH MoKeT pacIeIIJIaTBcra TpeOHnHdErHIpTa3Ob B IHTO3OJIe Do NH+ H-KeTOMacJIaHOH KNCJIoTBi, KOtOpa8 bICrpo H Heo6paTHMo pacIIaJaTeCra IO CO2; a TaKke OH MoKeT MeTA6OJIIN3HPOBaTcra TpeOHnHdErHIporeHa3Ou B MHTOXOHdPrHax Do aAMHHOaIeTOyKCycCHO KNCJIoTBi, KOtOpa 3aTeM o6paTHMo pacIIeIIJeTcra AMHHOaIeTOHCNTeTA3O JIO rLIInHa H aIeTIJI-KoA. IocJIeINHee MaIOBepoRTHO H3-3a KpaIHeH HeyCTOuHBOcTH N aAMHHOaIeTOyKCycHO KNCJIoTBi, KOtOpa IIpeKJe, Yem IIOIBeRrHyTcra DeIcTBHIO KaKOrO-JIN60 fepMeHTa, cAMIOIIpOH3BOJbHO DeKap6OKCHINPyETcRA B AMHHOaIeTOH, KOtOpbIK OKNCLIEcRA B aAMHHOaIeTOHOBOM IINKJIe DO KOHeuHBIX IPOJyKTOB.
B pa6oTe Moundras et al. [3] IOKa3aHo, YTo B TReIaTOuHTax Kpbicb 65% OKHcJIeHHr TpeOHHa
OCyIeCTBJIeTc
TJIHUNHHe3aBHCMBIM
TpeOHHHIeRnIpaTa3HBIM IyTeM -pacIIaI IIOI JeIcTBHeM TpeOHHHIeRnIpaTa3bI. IooJIhee House et al. [1] 2TO IOITBepINH CBOHMN HCCJIeIOBaHHaMn TaKKe c REIIaTOUHTaMH KpbICbl.
IockoJbky TpeOHnH YBJIeTcY He3aMeHHMOI aMHOKNCJIoToi, o6a fepMeHTa DoJIxKbI paCIIeIIITb erO yJIePoJHbI cKeJIeT Heo6paTHMo. EclH Heo6paTHMOCTb DeIcTBnA TpeOHnHdErHJaPaTa3bI He MoKet Bbl3bIBaTb COMHeHn, TO Heo6paTHMOCTb DeIcTBnA TpeOHnHdErHdpoReHa3bI HyKdaJIacb IIO HeJaBHeRo BpeMeHN B CIIeIHnAJIbHbIX DoKa3aTeJIbCTBax, T.K. JTeHdpoReHa3bI, KaI npABJIIO, DeIcSTByOT o6paTHMo. B IocJIeINHe roIbI Ha OCHOBaHH pa60t [4-7] Ioka3aHa Heo6paTHMOCTb DeIcTBnA TpeOHnHdErHdpoReHa3bI y MJIeKOIIHTaHOIIHX [8-11]. IIpHuEM B pa60te [5-7] B KaueCTBe o6beKta IJIa H3yueHn TpeOHnHdErHdpoReHa3bI HcIIIOJB3OBAJIHcB KpbIsI. TaKHM 6pa3OM, OIIbITb C KpbICaMH IpKO IeMOHcTpHyOT HEBO3MOKHOCTb CnHTe3a y MJIeKOIIHTaHOIIHX yJIePoJHOro cKeJIeTa TpeOHnHa, HNbIMH CJOBAMH, YTO TpeOHnHHe3aMeHHMa aMHOKNCJIoTa.
Bo3MoJxHocmb nepeamunupoabua mpeonuHa y Mlekonumaouux. KaK H3BeCTHO, eINHCTBeHHbIM IyTeM 6HoCnHTe3a He3aMeHNMBIX aMHNOHKNCJOT, KpOMe MeTHOHHa, y JKBOTHBIX JBJIeTc8 o6paTHMOe IIpeaMHHPoBAHHe KeToaHaJIOrOB 3THX aMHNOHKNCJOT C HeKOtOpbIM aMHNOHKNCJOTaM; MeTHOHIN MoKeT TaKKe IIOBepraTbC8 o6paTMOMy (B HTore) IpeMeTHJIHpOBaHHIO, paccMOTpeHHe KOtOpORo BbIXOJNT 3a paMKN cTaTbN.
Elliott H Neuberger [12] IpoBoJIH IBa 3KcIepHMeHTa.IIepBbIg 3KcIIepHMeHT 6blI IIpoBeJeH Ha KPOJIHKaX C OTHOCTeJIbHO MaJIbIM KOJIHecTBOM IJIINHa, coIepJkaIeero $^{15}\mathrm{N}$. BToPoJgKcIepHMeHT 6blI IIpoBeJeH Ha Kpbicax. B HEM KOJIInCeTBO $^{15}\mathrm{N}-$ IJIINHa 6blIO IOUTH B 4 pa3a BbIIIE, YEM B 3KcIepHMeHTe Ha KPOJIHKaX. BKJIIOueHHe $^{15}\mathrm{N}$ IIpi O'TOM 6blIO 3NaHTeJIbHO BblIE KaK B 6eJIkax BHYtpeHHIX OprAHOB, TaK H BO MHOHN XOTDeJIbHBIX aMHNOHKcIJOTax, Oco6eHHO B IJIINHe H o6pa3yIOIIeMcs H3 HeRo cepHHe, B To BpeMg KaK JIN3HN H TpeOHnH He IOKa3bIBaJI NOBbIIIEHHORo CoIepJkaHHa $^{15}\mathrm{N}$. OtCIOda Elliott H Neuberger [12] cIeJIaIH BbIBOD, qTO TpeOHnH, IIOIo6HO JIN3HNHy, He IIpHHMaet yuactHn B o6paTHMOM IpeHoce a3Ota, KOToPbI Ha6JIHOaETcY y dpyTHx aMHNOHKcIJOT, KaK 3aMeHHMbIX, TaK H He3aMeHHMbIX. DaHHbI cTepeOTHI CJOxIKJIcB TpAINHOHHoB 6HOxHMnH. TaK, B [1] ROBOpHTcR, qTO KJIeTKN MJIeKOIIHTaIOIIHX He 0BJIaIOT Heo6XoINHMbIMH $\phi$ ePMeHTaMH DJIa IpeaAMHHropOBAHn TpeOHnHa H IOCTyIIJIeHne 3Toi He3aMeHHMOI aMHOKcIJOTbI B KaTAbOJIInueckHe IyTuN IIpeCTaBJIeT ee Heo6paTHMyO IOTepIO IJIa CNHTe3a 6eJIka. B 3ToI pa6ote TaKke COo6IIaeTcR, qTO TpeOHnH- BTopra HIN TpeTBA JIMHTHPyoIIaam HHOKcIJOTA B IINTaHHn CBnHei, OCHOBAHHOM Ha 3epHOBo H CoeBOI IIHIIe, KaK COo6IIaIOcb BBIIe. IIpi 3ToM HnUeRO He ROBOpHTcR O JIMHTHPyoIIeM xapaKTpe TpeOHnHa IJIa KpbIC, Ha KOTopBX 6blIA BblIOJIHeHa daHHa pa6Ota.
Между тем Meltzer и Sprinson [13] показали, что после кормления крьс $^{15}$N-меченным лейцином очень малое количество $^{15}$N было обнаружено в трепонине, составляя только 2% такового, найденного в глутиаминовой кислоте, и менее 1%, выделенного в лейцине из тех же органов. В книге Майстера [4] на основании работ [12,13] делается вывод, что раз небольшое количество азота лейцина все же было обнаружено в молекуле трепонина, в организме животного происходит незначительный синтез трепонина или же реакции его расщепления частично обрата́мые. Майстер также не исключает, что отмеченное включение изотопного азота в трепонин, возможно, обусловлено действием микрофлоры кишечника. Но если бы последнее имело место, то столь же малое количество азота лейцина было бы обнаружено и в лизине, а этого не наблюдалось [13]. Майстер исключает образование трепонина из гомосерина в тканях животных. Невозможность синтеза трепонина из гомосерина у животных в XXI веке подтверждена Donini et al. [15].
T.T. Bepezov в своей монографии в 1969 г. указал как на доказанный факт, что в тканях мlekопитающих механизм переаминирования является и главным путем дезаминирования L-аминокислот и перечисляет все аминокислоты, участвующие в этом процессе [16]. Среди аминокислот T.T. Bepezov называет треонин, но не называет лизин, следовательно, он имеет в виду сами аминокислоты, а не продукты их превращения, потому что продукт превращения лизина — α-аминодиппиновая кислота — активно подвергается переаминированию. T.T. Bepezov в своей работе [16] также отмечает, что переаминирование может происходить в тканях между разнообразными монокарбоновыми донорами и акцепторами аминогрупп без участия дикарбоновых аминокислот. К реакциям этого типа относятся процессы переаминирования между рядом аминокислот и пировиноградной кислотой с образованием алианина и соответствующих α-кетокислот, протекающие в митохондриях. Была показана и обратимость этих реакций, а также различная способность отдельных тканей катализировать описанные превращения. Дальнейшие исследования подтверждают возможность переаминирования треонина у крыс. Так, в работе Noguchi T. et al. [17] рассматривается фермент серин-пируватаминотрансфераза, выделяемый из митохондрий печени крыс и катализирующий переаминирование различных аминокислот как с пировиноградной, так и с фениллировиноградной кислотой. Причем если фениллиранция весьма активно переаминируется серин-пируватаминотрансферазой с пировиноградной кислотой, то лейцин (в большой степени), треонин (в меньшей степени) и глицин (в очень малой степени) переаминируются ею только с фениллировиноградной кислотой (схема 1).
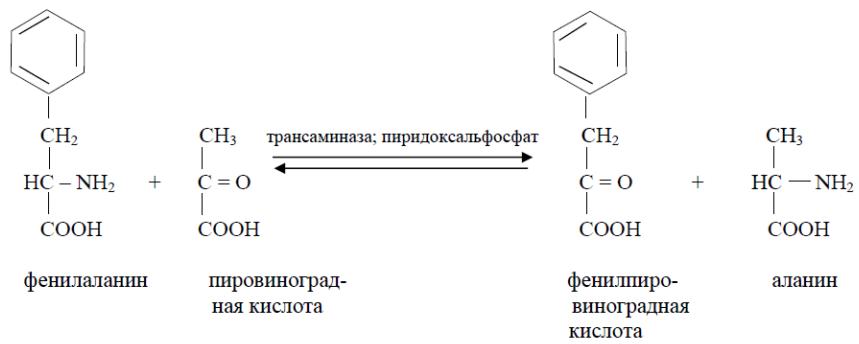
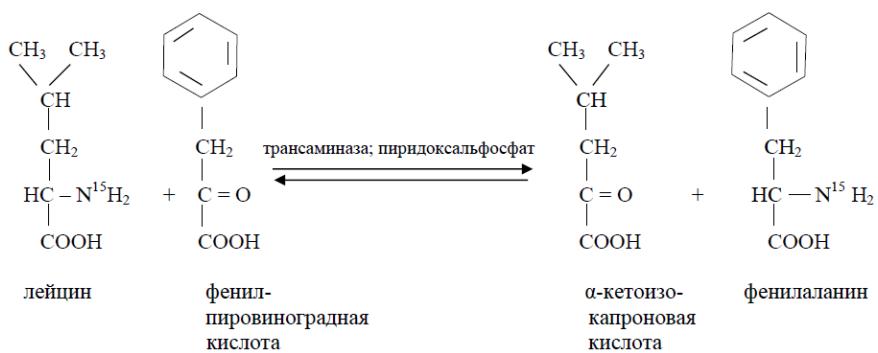
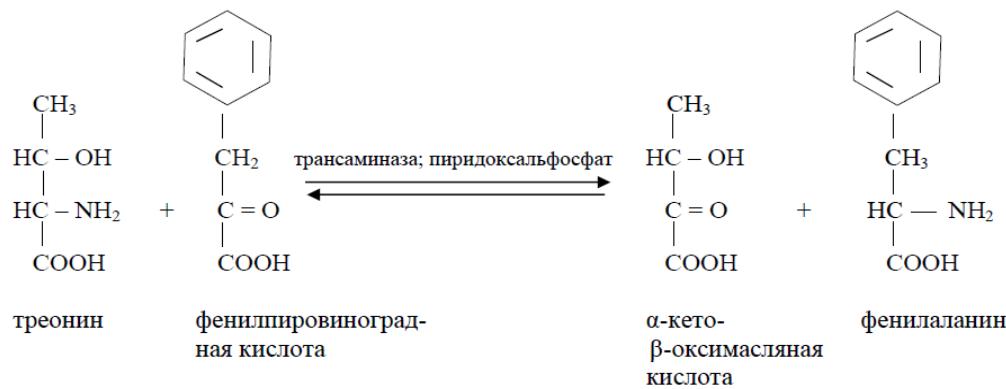
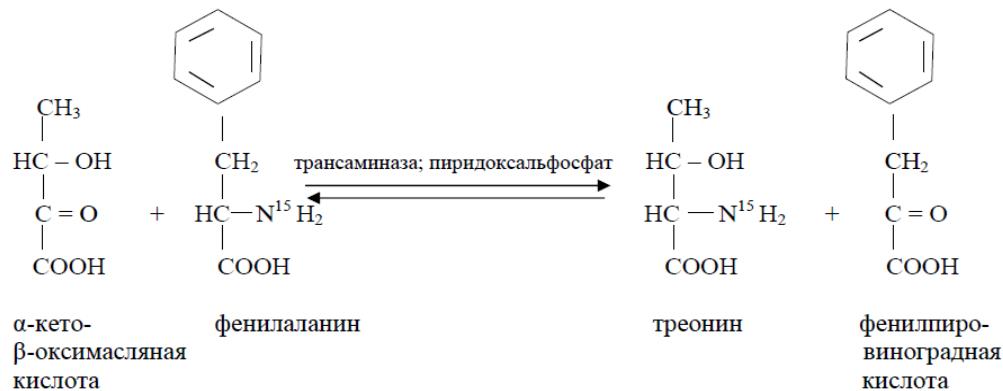
Cxema 1: O6paTHMOe IpeaAMHHPOBaHHe JeIiHa H TpeoHHa C fEHJINHPoBHHOrpaIHOH KHCJIoToH.
В работе Ishikawa et al. [18] устанавливается идентичность кинурунинаминотрансферазы почек и мозга крыс. Что касается субстратной специфичности обоих ферментов, то кроме кинурунинна (продукт распада триптофана), они способны катализировать переаминирование многих аминокислот как с пирониноградной, так и с фениллировиноградной кислотами. Однако если кинурунинаминотрансфераза мозга хорошо пераминирует почти все аминокислоты, то фениллировиноградной кинурунинаминотрансферазы почек не пераминирует с ней некоторые аминокислоты. Тренин пераминируется с фениллировиноградной кислотой обеими кинурунинаминотрансферазами, но в почках в небольшой степени, а в мозге так же активно, как и другие аминокислоты, уступая лишь метионину. С пирониноградной кислотой обе кинурунинаминотрансферазы пераминируют только ароматические аминокислоты. На лизин обе кинурунинаминотрансферазы не действуют, что подтверждает отсутствие у него способности к пераминированию. Следовательно, катализируемое кинурунинаминотрансферазой активное переаминирование с фениллировиноградной кислотой различных аминокислот, включая тренин, подтверждается мысль Т.Т.Березова, о том, что в тканях мелекопитающих оно является главным путем дезаминирования L-аминокислот [16]. Barret [19] отмечает, что мелекопитающим, большим уремией и находящимся на низкобелковой диете, давали α-кетокислоты — производные незаменимых аминокислот. Последние синтезировались в организме путем пераминирования. Оказалось, что в виде аминокислот необходимо давать только лизин, для которого отсутствует трансаминаза. В то же время степень использования α-кетокислот для синтеза соответствующих аминокислот различается. Валин, лейцин, изолейцин, метионин и фенилаланин быстро синтезировались путем пераминирования, в то время как гистидин, треонин и триптофан синтезировались в меньшей степени, а синтеза лизина вообще не наблюдается. В свете этого легко объясняется указанный выше следующий факт. Когда кроликов и крыс снабжали рационом с 15N меченным глицином, в тренине эта метка не включалась: в организме мелекопитающих треонин из глицина образовывался не может, а пераминирование подвергается лишь очень незначительная часть глицина. В то же время, обнаружение в треонине 15N, введенного в организм крыс с лейцином, есть результат пераминирования, которому активно подвергается лейцин и слабо подвергается треонин [19]. Следовательно, обнаружение в треонине (но не в лизине) 15N, введенного в организм крысы с лейцином, могло быть только результатом пераминирования.
CToHT TaKKe o6paTHb BHMaHHe, YTO T.T.Bepe3OB B [16] cHTaET, YTO 1e3aMHHHpOBAHHe тритофана осуществляется через разрыв индольного ядра с образованием кинурурина и далее 3-оксинурурина, которые или подвергаются перезаминированию с α-кетоглутаровой кислотой, или распадаются под действием специфической кинуруриназы с образованием аланина. Дезаминирование аланина так же происходит путем перезаминирования. Но в [19] зафиксировано перезаминирование тритофана в количестве, соизмеримом с треонином (по последним данным из всех природных аминокислот только лизин не способен подвергаться перезаминированию [19,20]). Из этого можно сделать заключение, что имеется в перезаминировании аминокислот вида аминокислота, а у крьс треонин подвергается перезаминированию, а у свиней не подвергается (в литературе сведения о перезаминировании треонина у свиней полностью отсутствующий, что обусловливает у последних его лимитирующий характер наряду с лизином и тритофаном при характерном для свиней зерновом питании. Исследования, проведенные Mastellar et al. [21], отрицают лимитирующий характер треонина для лошадей, что наводит на мысль о вероятном перезаминировании треонина у лошадей.
## II. Oco6eHHOCTHIpeBpaIeHnTpeOHnHa yJeJIOBeKa
Oco6eHHocMu kama6oU3Ma mpeOnHa y yeIOBeKa. Zhao et al. [22] He ydaIOcb 6hApuykHTb y yeIOBeKa cKOJIbKOHN6yIb 3aMeTHOrO IIpeBpaIeHnA TpeOHnHa Ila3Mb KpOBn B IINIIN. Edgar B CBOeI pa60Te [23] IpoBOiHT cpABHeHne REHOB TpeOHnHDeIrpOReHa3bl YeIOBeKa n pyJa XHBOTHbIX H DeJIaET BbIBO, YTO YeIOBeK B IpoIeCce EBOJIOIH N ytpaTHJI CNOCo6HocTb K CnHTe3y TpeOHnHDeIrpOReHa3bl. CJeIOBaTeJIbHO, Heo6paTMbI paIIaI TpeOHnHa IIO DeIcTBHeM TpeOHnHDeIrpTa3bl - eINHCTBeHHbI PyTB KaTaoJIH3Ma TpeOHnHa y yeIOBeKa, YTO coRIacyeTcA c H3BecTHbIM $\phi$ aKTOM, YTO TpeOHn HJIy YeIOBeKa - He3aMeHHmaj IJIOKOrEHHa amHHOKcJIoTA H YTO a-KeTOMacIJHnA KHcIJOTA - IpeIIEcTBeHHNK IJIOKO3bl.
BbIIeH3IIOKeHHoeJIeKoO6bIcHReT BpeI N36bITKa TpeOHnHa B IIHTaHHN DJIpaCTyUHx KpbicrT Ipr eTOcYtCTBnI DJIaJIeHIIeB. HMeIOIIaIcRy JxHBOTbIX TpeOHnHJeIHIporeHa3a OKcJIaeT (y IITnB 60JIbIIeMpe, y MJIeKOIIHTaIOIIHX-B Mehblie) TpeOHnH B aAMHOaIeTOYKcCHyIO KHCJIoTY, KOtopaI caMOIIPOHN3BOJIbHO Dekap6OKCHJIHpyeTCRy B aMHOAIIeTOH, OKcJIaIOIIncra Do KOHeuHbIX IpoJyKTOB B aMHHOaIeTOHOBOM IINKJIe. Ho B aAMHHOaIeTOYKcCHyIO KNCJIoTy IOI DaIeCTBHeM $\oint$ epMeHTa aMHHOaIeTOHcHNTeTa3bI TaKKe IpeBpAuaetcRgJINH IIyTeM KOJIeHCAIIH c aIeTHJI KoA. TaKIM o6pa3OM, y MJIOIIHTaIOIIHX, IaJce ecJH He IpoHCxoIHr IpeBpaIeHne TpeOHnHa B rJInHH [24,25], 3TN IBe aMHHOKHCJIoTBi KOHKypuyot 3a OKcJIeHHe B aMHHOaIeTOHOBOM IINKJIe. I36bITOK TpeOHnHa IIpHBOHr K rHIpePJIINHemHH co BCEMN BbITEKAIOIIHMn IocJIeCTBnHMn. HaH6OJIee rPo3HOe OCJIOXHeHne RHIpePJIINHEmHH-IOueHOKaMeHHa
6OJIe3Hb, BbI3BaHHa OKNCJIeHHem TJIINHnBa B IIaBeJeayUo KHCJIoTy H OTJIOKeHHe ee coJIe B IIOuKax. Y JIOHei ToKe ecTb aMHHOaIeTOHObB IIKJI N aMHHOaIeTOHcHHTeTa3a, IpeJHa3HaueHHbIe IJIa OKNCJIeHHa TJIINHnHa, HO oTCyTcTByET TpeOHHHIeRHaIporeHa3a. CJIeIOBaTeJIbHo, H36bIToK TpeOHnHa He MoJcET IprHBODITb K rHIeprJIINHHemHH.
Bo3MoJxHocmb nepeamunupo6aHn mpeonHua y yeIOBeKa. B IIOJIb3y IIOcJIeIHeRo rOBOpHT TOT $\phi$ aKT, YTO 6OJIee IIOJyBeKa Ha3aJ yCTaHOBJIeHO IHCTHTyTOM IIITaHNr AMH CCCP IIOI pyKOBOCTBOM aKaIDEMNka A.A. IIOKPOBCKORO, YTO IJIa YeIOBeKa H3 8 He3aMeHHMbIX aMHOKNCJOT JHMHTpyUOIMNH JBIAHOTc JIN3HH, MeTHOHIN H TPhIIToΦaH. CToHT KpATKO paccMOptPetb KaTa6OJIIN3M 3THX aMHOKNCJOT y YeIOBeKa, YTO6bI cpaBHInTB c KaTa6OJIIN3MOM TpeOHnHa.
JIIN3HH - eINHCTBeHHa H3 IIpHPOIHBIX aMHNOKHCJLOT, He cIIIOco6Ha IIOBHePraTbcIpeaMHNHPoBAHHO, a IOTOMy y IIO3BOHOUHbIX Heo6paTHM He ToJIbKO paIaN yIIEpoIHOrO cKeJIeTa JIN3HHa (KaK y BCEx IpyTHX He3aMeHNMBIX aMHNOKHCJLOT), HO IN De3aMHNHPoBAHHe 3TOI aMHNOKHCJOTbl. 3THM O6bAcHJaETcJIHMHTpyIOuH XapaKTep JIN3HHa IJIy HeJIOBeka.
B HaCTOJIiEe BpeM yCTaHOBJIeHO, YTO H3 cyIeCTByIOUHX B OprAHH3Me IIO3BOHOUHbIX YeTbIpex IyTei paIIaJa TPhIToΦaHa B HopMe 95% EToI aMHNOKHJIoTB Heo6paTHMo paIIaJaETcR IO KHNHyperHOBOmy IyTH [26, 27]. IocKoJIbky U YeJIIOBeKa B cNlIy erO IcnXnueckoi DeIeJIbHOCTH 3NaHTeJIbHO 6OJIbIIaay TaCtB, YEM y KOrOJIbHO H3 JKNBOTHbIX, OCTaBIHIXc 5% TPhIToΦaHa TaK JKe Heo6paTHMo pacXoIyETcRa Na Obo3OBaHHe cepOTOnHHa N yK COBCem He3NaHTeJIbHa aCtB Iekap6OKcHJInpyETcR B ΦH3NoILOrHuYeCKn aKTHBHbI TPhITaMHN, BpIa JIN CTOH TROBOpHTb O KOJIInueCTBe TPhIToΦaHa, IIOBepraHOIIeOcR
6paTHMOMy IpeaAMHHPOBaHHIO.CJIeIOBaTeJbHO,KaK y JIN3HHa, HAJINIO JINMMTHpyUOuN XapaKTep TpHITOTofaHa.
MeTHOHINJKe JERKO IODBepraeTcI
IIpeaMHINPOBAHIO, HO B OTJIHHe OT IpyTHX
He3aMeHHMBIX aHHOKNCJOT IIIA HrO, KpOME
IIpeaMHINPOBAHnia, XapaKTepHa N Ipyra peakiiu
OBpaTMOROPacIIaJa- IIpeMeTHJINPOBaHne. IIpHuem BCE
coeHNHeHn, IIOJIyuaIOIIHe y MeTHOHnHa MeTHJIbHyO
rpyIIy, He cIOco6HbI ee OTdABatb (peMeJIINPOBaHne
obpa3OBaBIIeFOscR TOMOUnCTeHNa B METHOHnH
OCUYIECTBJIaeTcRAIByMn, H3 KOtOpbIX OINH Tpe6yET
BHTaMHNa B12 H o6bIacHJeKPOBeTBOPHOe JeCHTBHe
IOcJIeIHero, HO paccMOtpeHne 3THX IIpoIeCCOB BIXoIHNT 3a
paMKn CtaTbN; B TO JxE BpeMa CJeIyEt OTMeHTb, YTO
BHTaMHN B12 B JxHBOTHom OPraHn3Me Tpe6yETcB KaueCTBe
KoΦePeMeHTa ToJIbKO DIA 2 peaks, KOtOpbIe Obe HmEOT
OTHOIIeHne K IIpeBpaIeHNo aMHNOHKNCJOT, HO K
KpOBetBOpeHHIO-OhNA). K TaKM CoeINHeHNM OTHCHTc
KpeaTHN. EcJIn yueCtB, YTO 3a cyTK NeIOBek BblJeIeT C
MoOy B CpeINhem 1,5 r KpeaTHHHa- IIpoDyKTA
Heo6paTMOROp pacIIaJa KpeaTHHa, TO CTaHOBTcA
IOHAYTHBM JIMMHTHPyOIIH xapaKTEp MeTHOHnHa.
B To JKe BpeMn HHKaKHX CBHJeTeJIbCTBOJHMHTpyHOWeM XapaKTepe TpeOHHa JJIa YeJIObeka HeT.3To MoKeT TOBOpHTb TOJIbKO 6o6paIeHHn pacIIaJaTpeOHHa, ToecTho eTO IpeeaMHnPoBaHH.
В работе [28] сообщается о кинурениаминотрансферазе, полученной из печени человека. Этот фермент оказался идентичным серин-глиоксилатаминотрансферазе. В отличие от серин-пируватаминотрансферазы крис он катализирует пераминирование ряда аминокислот с пиронингидронной, но не с фенилпировиноградной кислотой, причем треонин с ней пераминируется в небольшой степени (схема 2):

Cxema 2: IpeaMHnHPOBaHHe TpeOHHa c IInpOBHHoIpaIHoi KHCJIoToB V IIeueHN YeIOBeKa.
B pa6oTe [29] paccMaTpHbAIOTCaMHHO aHHaT aHHOTpaHcΦepa3bI I N II PeueHH YeJIOBeKa. O6a ΦepeMeHTa cIIOco6HbI KaTaJIH3HpOBA Tb 06paTHMOe IpeeaMHnPOBaHHe c α-KeTOrJyTapoBOH KHCJIoTOH He только α-аминoadипиновой кислоты, но и природных аминокислот, а также кинуренина и орнитина (продукта распада аргинина). Если в отличие от амино адипат аминотрансфераза II амино адипат аминотрансфераза I
He JeHCTBOBaJa Ha TpHIToΦaH H KINHypeHH, To Ha OctaJIbHbIe aMHHKNCJIoTbI, B TOM YHCJIe TpeOHHH,
IeICTBOBaJIH o6a $\phi$ epMeHTa B OJHHaKOBO He6OJIbIIIOI CTeIeHH (cxema 3):
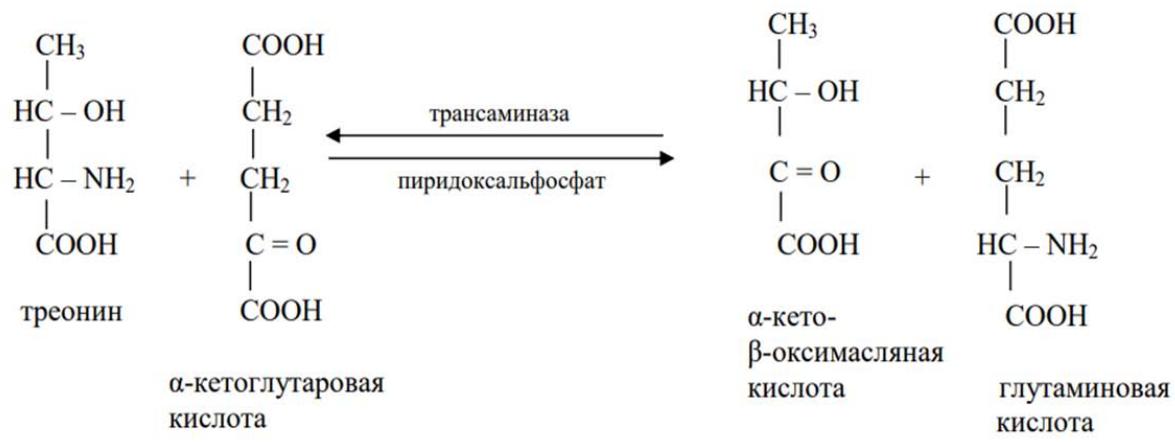
Cxema 3: IpeaMHHPOBaHHe TpeOHHa c $\alpha$ -KeToIyTapoBoi KHCJIoToB I NeueHH YeIOBeKa.
Работа [30] специально посвящена субстратной специфичности кинуренинаминотрансферазы II, выделенной из мозга человека. Кинуренинаминотрансфераза оказались идентична аминоадипатаминотрансферазе. Хотя этот фермент активнее всего катализирует переаминирование кинуренина и α-аминодипиновой кислоты с α-кетоглутаровой кислотой, он обладает широкой субстратной специфичностью и способен переаминировать 16 аминокислот с 16 α-кетокислотами. Среди первых называется и треонин, но среди вторых его кетоаналог не называется. Из этого можно сделать вывод, что α-кето-β-оксимасляная кислота, будучи химически неустойчивым соединением, быстро (но обратимо) восстанавливается в α, β-дигидроксимасляную кислоту с помощью НАДН или НАДФН и соответствующей дегидрогеназы и потому в организме не обнаруживается.
Itak, oTCyTcTBne JHMHTpyHIOeero XapaKTepa TpeOHnHa IJIa YeIOBeka IIpH IIpeo6JaIaHHN 3epHObIX B paIHNoHe MoKeT O6bXcHrTbcr ToJIbKO 6paTHMocTbIO HaJbHorO 3TaIIa eRo KaTAb0JIH3Ma-IEpeAMHHPOBaHHa, KOTOpoe y YeIOBeka HMeet MeCTo. CToNT 6paTHTB BHMaHHe, YTO TaKHe He3aMeHHMbIe aMHNOHKcIJOTbI, KaK JeIiHH, I3OJIeIiHH, BaJIHH N fEHNJIAJIaHHN He ABJIHOITcI IJIa YeIOBeka JINMMTHpyIOUHHa, a BCE OHN JERKO IIOBBePraOTcI IpeaAMHHPOBAHHIO. O BBICOKo cNOC6HocTH fEHNJIAJIaHHa K IpeaAMHHPOBAHHO HapJyC JeIiHHOM, I3OJIeIiHHOM H BaJIHHOM rOBOPHT TO fKaKT, YTO fEHNJIAJIaHHN YBJIeTcR eHNCTBEHHO INIKJIuYeCKoA MHHOKHCJIoTOI, KOtopyIO IIpH ypeMHN 3aMeHJIOET ee A-KeTOaHaJIOROM B DHeTe [31]. Heo6xoJIMO OTMeHTb, YTO ecJIN IJIeIiHHa, I3OJIeIiHHa H BaJIHHa IpeaAMHHPOBAHHe JBIAeTcR eHNCTBeHHbIM IyTeM IH KATA6OJIH3Ma, TO kATA6OJIH3M fEHNJIAJIaHHNa B 3IOPOBOM opraHH3Me B OCHOBHom 3aKJIIOuaeTcR B HEo6paTHMOM OKHCJIeHHN B THPO3HH, YTO HNKaK He IIPOTHBopeYHT BBICOKo CIOOC6HocTH fEHNJIAJIaHHHa K
ИпеаМНноПОБАHHО. Даже в ИНХМТНПЮОУЯДЛЯЧЕЖИОБЕКА АМХНОКХЦИОТА МЕТОХ, КАТАНХЗМ КОТОРОГО ВИПКАТЕЦБ НЕОБРАЩАТЕ ЦЕПБ ИЖЯ IIПЕВПАЙЕННА ЦЕПНА В ИНЦТЕХН, АКТНВО ИОДБЕПРЕЦИ ИПЕАМННПОБАHHО, ОЖЕМРОБОПИОЦБИИЕ. ТОТАК ЖЕ КАК ИООБЖОЙАЕТ IIПХ ЮПЕМН 3АМЕХЯР БМЕТОХ Н6ЕЗА3ОТНЦТБИМ АНАИОРМ БДХЕТЕ[29]. АХАИОТУХО КАТАЗОЖИЗМ ТПЕОХНА В ОПРАХЗМЕ ЕЖИОБЕКА 3АКЖИОУАЕЦБ И НЕОБРАЩАТЕ ЦПЕОХНА ИОДБЕЦТВХ ТПЕОХНДИГХПАТА3БИ, ЫТО ХНКАК НЕ ИПОТХБОПЮНТ ИПЕАМННПОБАHHО КОТОПОТО КОЖИНЕЦТАБА ТПЕОХНА.
Но какова же суточная потребность человека в тренине? Давно установлено, что 0,5 г тренина в сутки является минимальной дозой, обеспечивающей азотистое равновесие. Однако количество, гарантирующее азотистое равновесие, у каждой незаменимой аминокислоты должно быть выше в 2 раза этого минимума. Следовательно, для тренина оно будет 1 г в сутки. В то же время академик А.А. Покровский считал, что оптимальное количество белка и незаменимых аминокислот в питании должны не только поддерживать азотистое равновесие, но и обеспечивать сопротивляемость организма к инфекциям и другим вредным агентам внешней среды, способствовав улучшению здоровья и повышению работоспособности. Он предложил 2-2.7 г тренина в сутки. Примечательно, что ФАО предложено весьма близкое количество тренина в сутки-2.8 г. При этом содержание тренина в большинстве рационов доходит до 3 г в сутки, поэтому говорить о его лимитирующем характере для человека не приходится.
## III. 3aKJIIOueHHe
EcJIN IJIY BCEX HCCJIeIOBAHHbIX BHNIOB IIO3BOHOUHbIX, BKJIIOUa YcIIOBeKa, He3aMeHNMBIMN YBJIHOITc8 aMHNOKNCJIoT, TO JINMHTpyIOUIN XapaKTep TOI HJIN HHOJ He3aMeHNMOJ aMHNOKNCJIOTB MoKeT OTJNUATbc8 y pa3JIuHbIX BHNOB. Ha Hero MOryt BJINrTb pa3JIuHbIe fKaTOpbI: coJIepKaHHe daHHoJ aMHOKnCJIoTBi B paIHHOHe, cIOco6HoCTb K o6paIeHIO HauJIbHbIX peakHn KaTa6OJIH3Ma, pacXoJ ToH JIn HHOJ aMHOKnCJIoTBi Ha o6pa3OBAHne $\phi$ h3HOJIOrHueckn AKTHBbIX coeINHeHn I np. B DaHHoJ pa6Ote Ha 6HOXMnueckOM ypOBHe IOKa3AHbI IIpHuHNbI JHMHTpyIOIeTO XapaKTepa TpeOHHa IJIa CBHHeN OTCyTcTBn ETO rXapaKTepa IJIa YeJOBeKa, a TaKKe IIpoaHaJIH3NPOBaHbI pa3JIuHbIe IIpHuHNbI JHMHTpyIOIeTo XapaKTepa ToI HIn HHOJ He3aMeHmO aMHOKnCJIoTBi, UTO IIpeIcTaBJIeT CO60 BoJIbIIyU BaJxHOCTb IIpr COCTaBJIEHN paIHHOHB.
### JIHTepaTpa
1. House J.D., Hall B.N., Brosnan J.T. Threonine metabolism in isolated rat hepatocytes. Am. J. Physiol. Endocrinol. Metab. 2002, 281: E 1300-E1307.
2. Chapman K. The impact of the splanchic bed on the dietary requirements of threonine and lysine in humans, Canada, University of Toronto, 2011.
3. Moundras C., Bercovici D., Remesy C., Demigne C. Influence of glucogenic amino acids on the hepatic metabolism of threonine. Biochem. Biophys. Acta. 1992; 1115 (3): 212-219.
4. Laver W.G., Neuberger A., and Scott J.J. $\alpha$ -Amino- $\beta$ -keto-acids II. Rates of decarboxylation of the free acids and the behaviorer of derivates on titration. Journal of the Chemikal Society. 1959: 1483-1491.
5. Pagani R., Guerranti R., Leoncini R. and Marinello E. Activation and inhibition of rat liver L-threonine dehydrogenase. Ital. J. Biochem. 1990; 39: 108.
6. Pagani R., Guerranti R., Righi S., Leoncini R., Marinello E. and Pizzichini M. Identification of a mitochondrial inhibitor of rat liver L-threonine dehydrogenase. Biochem. Biophys. Acta. 1995; 1244: 49-52.
7. Guerranti R., Pagani R., Neri S., Errico S.V., Leoncini R. and Marinello E. Inhibition and regulation of rat liver L-threonine dehydrogenase. By different fatty acids and their derivates. Biochem. Biophys. Acta. 2001; 1568: 45-52.
8. Malinovsky A.V. Is threonine an essential amino acid? Collection of scientific papers of the Saint-Petersburg State University. Series 3: Biology. 2011; 1: 72-78.
9. Malinovsky A.V. Reason for indispensability of threonine in humans and other mammals in comparative aspect. Biochemistry (Moscow).2017; 82 1055-1060.
10. Malinovsky A.V. Why Threonine Is an Essential Amino Acid in Mammals and Birds: Studies at the Enzyme Level. Biochemistry (Moscow).2018; 83: 795-799.
11. Malinovsky A.V. Reasoning of generation of threonine indispensability in evolutionary aspect.
- with alanine-glyoxylate aminotransferase and serine-pyruvate aminotransferase. Biochem. J. 1980; 189: 581-590.
29. Okuno E., Tsujimoto M., Nakamura M. et al. 2-Aminoadipate-2-oxoglutarate aminotransferase isoenzymes in human liver: a plausible physiological role in lysine and tryptophan metabolism. Enzyme Protei. 1993; 47: 136-148.
30. Han C., Cal T., Tagle D.A. et al. Substrate specificity and structure of human aminoadipate aminotransferase/kynurenine aminotransferase II. Biosci.Rep. 2008; 28: 205-216.
31. Malinovsky A.V. Essential amino acids and their $\alpha$ -keto- and hydroxyl analogues in the diet of uremic patients (biochemical aspect). Clinical Nephrology. 2022; 14: 94-101.
Generating HTML Viewer...
References
31 Cites in Article
J House,B Hall,J Brosnan (2002). Threonine metabolism in isolated rat hepatocytes.
K Chapman (2011). The impact of the splanchic bed on the dietary requirements of threonine and lysine in humans, Canada.
Corinne Moundras,Daniel Bercovici,Christian Rémésy,Christian Demigné (1992). Influence of glucogenic amino acids on the hepatic metabolism of threonine.
W Laver,A Neuberger,J Scott (1959). 287. α-Amino-β-keto-acids. Part II. Rates of decarboxylation of the free acids and the behaviour of derivatives on titration.
R Pagani,R Guerranti,S Righi,R Leoncini,D Vannoni,E Marinello (1990). Rat liver L-threonine dehydrogenase.
R Pagani,R Guerranti,S Righi,R Leoncini,E Marinello,M Pizzichini (1995). Identification of a mitochondrial inhibitor of rat liver L-threonine dehydrogenase.
R Guerranti,R Pagani,S Neri,S Errico,R Leoncini,E Marinello (2001). Inhibition and regulation of rat liver L-threonine dehydrogenase by different fatty acids and their derivatives.
V Shaidulin,D Milanov,A Rusakov,A Veselova (2011). Determination of themean orbit for meteoroid streams.
A Malinovsky (2017). Reason for indispensability of threonine in humans and other mammals in comparative aspect.
A Malinovsky (2018). Why Threonine Is an Essential Amino Acid in Mammals and Birds: Studies at the Enzyme Level.
A Malinovsky (2019). Reasoning of generation of threonine indispensability in humans and mammals in evolutionary aspect.
D Elliott,A Neuberger (1950). The irreversibility of the deamination of threonine in the rabbit and rat.
Herbert Meltzer,David Sprinson (1952). THE SYNTHESIS OF 4-C14, N15-l-THREONINE AND A STUDY OF ITS METABOLISM.
А Майстер (1961). Биохимия аминокислот, Иностранная литература.
Stefano Donini,Riccardo Percudani,Alfredo Credali,Barbara Montanini,Andrea Sartori,Alessio Peracchi (2006). A threonine synthase homolog from a mammalian genome.
Т Березов (1969). Обмен аминокислот нормальных тканей и злокачественных опухолей. Медицина.
T Noguchi,E Okuno,R Kido (1976). Idenity of isoenzyme 1 of histidine-pyruvate aminotransferase with serinepyruvate aminotransferase.
T Ishikawa,E Okuno,M Tsujimoto,M Nakamura,R Kido (1991). Kynurenine-Pyruvate Aminotransferase in Rat Kidney and Brain.
G Barret (2012). Chemistry and biochemistry of the amino acids.
Jinhan Yu,Andrea Daru,Min Deng,Donna Blackmond (2018). Prebiotic Access to Enantioenriched Amino Acids via Peptide-Mediated Transamination Reactions.
S Mastellar,A Moffet,P Harris,K Urschel (2016). Effects of threonine supplementation on whole-body protein synthesis and plasma metabolites in growing and mature horses.
X Zhao,Z Wen,C Meredith,D Matthews,D Bier,V Young (1986). Threonine kinetics at graded threonine intakes in young men.
A Edgar (2002). The human L-threonine 3dehydrogenase gene is an expressed pseudogene.
M Hilliar,N Huyen,C Girish,R Barekatain,S Wu,R Swick (2019). Supplementing glycine, serine, and threonine in low protein diets for meat type chickens.
Shemil Macelline,Peter Chrystal,Sonia Liu,Peter Selle (2022). Implications of elevated threonine plasma concentrations in the development of reduced-crude protein diets for broiler chickens.
A Badawi (2017). Unknown Title.
A Badavi,Egypt (2019). International Journal of Basic & Clinical Pharmacology.
Etsuo Okuno,Yohsuke Minatogawa,Masayuki Nakamura,Naoki Kamoda,Junko Nakanishi,Minoru Makino,Ryo Kido (1980). Crystallization and characterization of human liver kynurenine–glyoxylate aminotransferase. Identity with alanine–glyoxylate aminotransferase and serine–pyruvate aminotransferase.
Etsuo Okuno,Moriyuki Tsujimoto,Masayuki Nakamura,Ryo Kido (1993). 2-Aminoadipate-2-Oxoglutarate Aminotransferase Isoenzymes in Human Liver: A Plausible Physiological Role in Lysine and Tryptophan Metabolism.
Qian Han,Tao Cai,Danilo Tagle,Howard Robinson,Jianyong Li (2008). Substrate specificity and structure of human aminoadipate aminotransferase/kynurenine aminotransferase II.
Malinovsky Malinovsky (2022). Essential amino acids and their α-keto- and hydroxy analogues in the diet of uremic patients (biochemical aspect).
No ethics committee approval was required for this article type.
Data Availability
Not applicable for this article.
How to Cite This Article
A.V. Malinovsky. 2026. \u201cBiochemical Reasons for the Presence of the Limiting Character of Thrheonine in Some Mammals and the Absence of the Limiting Character of Threonine in Humans\u201d. Global Journal of Medical Research - G: Veterinary Science & Medicine GJMR-G Volume 23 (GJMR Volume 23 Issue G1).
Explore published articles in an immersive Augmented Reality environment. Our platform converts research papers into interactive 3D books, allowing readers to view and interact with content using AR and VR compatible devices.
Your published article is automatically converted into a realistic 3D book. Flip through pages and read research papers in a more engaging and interactive format.
Our website is actively being updated, and changes may occur frequently. Please clear your browser cache if needed. For feedback or error reporting, please email [email protected]
Thank you for connecting with us. We will respond to you shortly.
Lorem ipsum dolor sit amet, consectetur adipiscing elit. Ut elit tellus, luctus nec ullamcorper mattis, pulvinar dapibus leo.
Biochemical Reasons for the Presence of the Limiting Character of Thrheonine in Some Mammals and the Absence of the Limiting Character of Threonine in Humans