Anny Kelly Rocha de Oliveira Ferreira", Bruna Lorrany Mariano Rodrigues, Dalila Estefânia Mariano Souza®, Elizabete Rocha de Oliveira Gonçalves, Ana Elizabeth Oliveria de Araújo Alves * & Marina Firmino Lima de Oliveira
Resumo- Introdução: O plasma rico em plaquetas (PRP) é uma fração líquida do sangue periférico, conhecido por sua concentração elevada de plaquetas e tem sido utilizado na medicina regenerativa devido ao estímulo de regeneração tecidual. Os fatores biologicamente concentrados, ativos e liberados pelas plaquetas, incluindo os fatores de crescimento, citocinas e proteínas de adesão, influenciam todas as etapas do processo cicatricial. Apesar dos avanços promissores, a variabilidade nos métodos de preparação apresenta desafios significativos para sua aplicação clínica.
Métodos: Trata-se de um relato de caso, realizado em uma clínica escola de um centro universitário privado do Distrito Federal, Brasil. Foram coletados dados clínicos do paciente de 67 anos com úlceras crônicas no tornozelo, mediante entrevista, fotodocumentação e assinado o termo de consentimento livre e esclarecido. Após concordância com a pesquisa, foram realizadas coletas de sangue em todas as sessões realizadas. O sangue total com 30 ml foram distribuidos em tubos de coleta com heparina e centrifugado a 1800 rpm por cinco minutos para obtenção de cerca de 8 ml de plasma total. Logo em seguida foi realizada uma assepsia simples no local a ser aplicado e adicionado o plasma total diretamente na ferida. O concentrado plasmático foi quantificado em relação a sua densidade. Foi realizado uma
Resultados: Observou-se uma melhora visível na cicatrização da úlcera após asprimeiras quatro sessões de tratamento com PRP, resultando em uma regressão cínica significativa. A paciente relatou sensações de repuxamento, dor, vermelhidão e formigamento durante o tratamento devido ao estímulo da cicatrização. É evidente o controle da inflamação com a diminuição da hiperemia e inchaço, afinamento e renovação do processo de quetatinização das bordas da ferida, finalizado com a diminuição acentuada da lesão tecidual. O protocolo de aplicação foi rigorosamente aplicado em todas as sessões para obter uma base na qual descreveria um protocolo padrão.
Conclusão: Os resultados destacam o potencial do PRP como uma terapia eficaz para promover a cicatrização de úlceras. Pacientes em situações crônicas, comorbidades de difícil controle, farmacoterapia ineficaz, e outras condições ambientais desfavoráveis, indicam este paciente como preferência para este tipo de tratamento, uma vez que o protocolo é simples e confortável, não exige gastos financeiros exorbitantes com coberturas usadas em curativos tradicioanis, e naõ afetam o estado de saúde geral do paciente. A pesquisa contínua nessa área é essencial para otimizar o uso clínico do PRP e melhorar os resultados de cicatrização em pacientes com essa condição complexa.
## I. INTRODUÇÃO
plasma rico em plaquetas (PRP) autólogo, a fração líquida processada do sangue periférico do próprio paciente, possui uma concentração de plaquetas superior ao nível basal e tem sido amplamente utilizado em diversos campos médicos ao longo dos últimos 30 anos(Everts et al., 2020).
A premissa científica por trás da terapia com PRP é que a injeção de plaquetas concentradas no local da lesão pode estimular a reparação tecidual através da liberação de numerosos fatores biologicamente ativos, como fatores de crescimento, citocinas e proteínas de adesão, que desempenham papéis cruciais na hemostasia, síntese de novo tecidoconjuntivo e revascularização. Embora as terapias com PP tenham mostrado benefícios clínicos promissores e resultados encorajadores, inconsistências nos resultados dos pacientes e a variabilidade dos métodos com uso do PRP apresentam desafios significativos para sua regularização prática. As técnicas de preparação variam amplamente, contribuindo para resultados inconsistentes. Além disso, a falta de uma padronização dos protocolos de preparação do PRP dificulta ainda mais a obtenção de resultados uniformes. Este artigo revisará os desenvolvimentos recentes na preparação do PRP, dosagens de plaquetas, concentrações de fatores de crescimento e citocinas, além de explorar o impacto desses elementos na regeneração tecidual e nos processos de cicatrização(Everts et al., 2020).
Segundo os estudos de Gupta et al. (2020), o PRP é composto por várias proteínas essenciais que auxiliam na cicatrização, além das fibrinas presentes no plasma. Entre essas proteínas estão o fator de crescimento transformador beta (TGF-β), os fatores de crescimento epidérmico e endotelial vascular (EGF e VEGF), os fatores de crescimento derivados de plaquetas (PDGF), os fatores de crescimento de fibroblastos (FGF), fatores de crescimento semelhantes à insulina (IGF-1), entre outros. O TGF- $\cdot \beta$, por exemplo, é secretado por plaquetas e macrófagos, desempenha um papel crucial na regeneração óssea e na cicatrização a longo prazo, além de inibir a atuação dos osteoclastos. Ele também participa no crescimento de células epiteliais e endoteliais vasculares e produção de colágeno. Os EGFs promovem a proliferação e diferenciação celular, desempenhando um papel essencial na angiogênese e na cicatrização. Os VEGFs estimulam a especialização de células precursoras em células endoteliais maduras e incentivam a formação de capilares sanguíneos. Os PDGFs surgem no local da lesão e ativam proteínas sinalizadoras que iniciam a mitogênese, angiogênese, ativação de macrófagos e produção de colágeno. Os FGFs também são importantes para a migração dos fibroblastos, produção de colágeno e reparação tecidual, bem como os IGF-1s são fundamentais no crescimento celular e na cicatrização. O fator de crescimento do tecido conjuntivo (CTGF) é uma proteína secretada que interage com outras moléculas, sendo altamente expressa durante a cicatrização de feridas e fortemente relacionada à angiogênese.
O concentrado de plasma rico em plaquetas apresenta cerca de 2 a 3 vezes mais comparado aos níveis basais encontrados no sangue total. O processo de preparação do PRP começa com a coleta de sangue por meio de punção venosa. Em seguida, a amostra é centrifugada, e o plasma enriquecido com plaquetas é extraído. Idealmente, a produção de PRP por meio de centrifugação com baixa aceleração de tempo é considerada benéfica, embora a evidência clínica ainda seja limitada. A centrifugação separa as hemácias do volume sanguíneo total, deixando as camadas superiores ricas em plaquetas e leucócitos, enquanto a camada intermediária (buffy coat) é especialmente rica em leucócitos. Para obter PRP puro (P-PRP), as camadas superiores são separadas do volume sanguíneo, incluindo uma parte rasa do buffy coat. Existem diversos sistemas de PRP aprovados pela
Food and Drug Administration (FDA) e pela Health Canada para uso na prática médica. As classificações do PRP são baseadas em diferentes critérios, como a presença ou ausência de leucócitos e fibrina, além da dosagem, eficiência, pureza e ativação do produto. Essas variações são importantes para definir o tipo e a qualidade do PRP utilizado em diferentes contextos clínicos (Gupta et al., 2020).
O PRP surge como uma terapia promissora, principalmente para pacientes diabéticos, especialmente aqueles propensos a úlceras nos pés devido às complicações da doença. Além de potencializar a formação de novos vasos sanguíneos e a produção de colágeno, o PRP pode acelerar a regeneração de tecidos e oxigenação tecidual, oferecendo uma alternativa significativa aos tratamentos convencionais. Em um contexto onde as úlceras crônicas representam um desafio sério de saúde, a pesquisa contínua e o desenvolvimento de terapias eficazes como o PRP são fundamentais para melhorar os resultados de cicatrização e, consequentemente, a qualidade de vida desses pacientes. Indivíduos com diabetes têm maior propensão a desenvolver feridas nos membros inferiores devido a problemas como neuropatia periférica, redução da circulação sanguínea e sistema imunológico comprometido. Essas úlceras frequentemente não respondem bem aos tratamentos convencionais, como trocas de curativos e controle da glicemia, resultando em feridas crônicas que cicatrizam lentamente. Elas são uma complicação séria do diabetes e podem levar a complicações graves, como amputações e maior risco de morte. Existem várias opções de tratamento para úlceras nos pés diabéticos, como desbridamento, enxertos de pele e revascularização. O PRP tem sido estudado como uma terapia promissora para esses pacientes devido à sua facilidade de obtenção e aplicação, bem como a capacidade de liberar fatores de crescimento que estimulam a formação de novos vasos sanguíneos, produção de colágeno e regeneração de tecidos, melhorando assim os resultados de cicatrização de feridas(Kunder et al., 2023).
Por essa razão, este trabalho tem como objetivos demonstrar o papel do PRP na cicatrização de feridas crônicas e promover a criação de um protocolo base. Embora o campo ainda enfrente desafios, avanços significativos têm sido feitos na compreensão da ação do PRP e seu impacto na regeneração tecidual. desenvolvimento de abordagens terapêuticas são cruciais para otimizar os resultados clínicos e melhorar a qualidade de vida dos pacientes diabéticos afetados por úlceras nos pés.
## II. MATERIAIS E MÉTODOS
Trata-se de uma pesquisa do tipo exploratória, descritiva por meio de relato de caso realizada de março a junho de 2024. O trabalho foi realizado em clínica escola de um centro universitário privado do Distrito Federal, localizado na região administrativa do Gama, sob a autorização CAAE: 64704322.0. 0000.5058. Para seleção do paciente foram adotadas os seguintes critérios de inclusão: pacientes com feridas crônicas, sexo masculino ou feminino, maior de 18 anos, em uso ou não de ativos para a melhora das feridas crônicas, que aceitem participar do projeto de pesquisa após assinatura do Termo de Consentimento Livre e Esclarecido (TCLE) e termos de uso de imagem; exame laboratorial de hemograma com data retroativa dos últimos três meses contendo: hematócrito > 45%, hemoglobina $>$ 15g/dL e contagem de plaquetas acima de $150.000 / \mathrm { m m } ^ { 3 }$. Os critérios de exclusão foram pacientes com dificuldade de locomoção, gestantes, tabagistas, etilistas, indivíduos com síndromes ou quadros psicóticos, imunodeprimidos e aqueles que estejam acometidos pelo vírus SARS-COV-2, pacientes com casos de distúrbio de coagulação, hemofilia, lesões neoplásicas, doença infectocontagiosa, uso contínuo de medicamentos anticoagulantes, antiplaquetários e transfusão sanguínea nos últimos três meses, pacientes com fobia a agulhas ou aqueles que se negarem a assinar os termos necessários para participação no estudo.
A paciente selecionada tem 67 anos, apresentava uma ferida aberta há aproximadamente três anos, com dimensões de 2 cm de altura por 4 cm de largura no momento da inclusão no projeto. Além disso, tinha uma segunda ferida já fechada, mas com sinais de inflamação e sensibilidade local, medindo 6 cm de largura por 3 cm de altura. Durante a entrevista, a paciente relatou que a ferida teve origem em um impacto contra um portão, inicialmente causando inchaço, dor local e inflamação, evoluindo para uma ferida aberta. Devido à gravidade, ela foi hospitalizada por cerca de dois meses, recebendo cuidados intensivos na UTI para tratar a infecção. Seu histórico clínico inclui hipertensão arterial, diabetes tipo 2, neuropatia e ansiedade, com uso diário deGlifagem, Gliclazida, Amiodarona e Fluoxetina. A paciente não mantém atividade física regular e possui hábitos alimentares pouco saudáveis. As úlceras da paciente estão localizadas no tornozelo, área comum para úlceras em pacientes com dificuldades de mobilidade, conforme protocolo de avaliação de feridas.
Na clínica escola, o paciente foi encaminhado à sala de procedimento. Foi realizada a assepsia ao redor da ferida com álcool $70\%$ e na ferida limpeza com clorexidina alcóolica, seguindo as regras de higienização de feridas de Olufemi, 2017. Esse procedimento de limpeza era realizado a cada retorno semanal do paciente. Após a coleta venosa, o sangue foi transferido para cinco tubos com hepatina e centrifugados a 1800 rpm por cinco minutos em um único ciclo. Após a centrifugação, o plasma foi separado, verificando-se a presença de agregados leucocitários e analisada a densidade sanguínea do plasma com um refratômetro.Em seguida aplicou-se o plasma enriquecido com plaquetas (PRP) diretamente nos locais afetados. Recomendou-se à paciente manter o curativo entre doze e vinte e quatro horas, sem removê-lo, além de evitar esforços físicos, ortostatismo prolongado e seguir corretamente a medicação prescrita pelo médico e buscar uma dieta saudável. Durante as aplicações, a paciente não apresentou desconfortos significativos. A fotodocumentação foi realizada por câmera digital do celular dos alunos pesquisadores.
Para a utilização do PRP, seguiu-se o método manual, aplicando-o diretamente na lesão por meio de pipeta milimetrada estéril. Depois de 3 min, a ferida foi ocluída com gazes impregnadas com o PRP e PRF, e finalizado com atadura.
### Protocolo Definido:
- Materiais: garrote, algodão, álcool $70\%$, scalp 21G, seringas de 5 ml, tubos com anticoagulante, devidamente identificados, gaze e atadura, centrífuga, densidômetro.
- Fotodocumentação em todos os ângulos, utilizando uma régua simples;
- Assepsia no local da punção: coleta sanguínea de 24 ml;
- Centrifugação: 1800 rpm, por 5 minutos.
- Quantificação da densidade total: seguiu-se a calibração do densidômetro com soro fisiológico estéril e a quantificação do plasma após centrifugação.
- Aplicação na região ulcerada: plasma rico em plaquetas foi aplicado na ferida, sendo espalhado em toda a área afetada, deixando a úlcera bem saturada antes de cobrir com o plasma rico em fibrinas para fechar o curativo. O curativo, realizado no laboratório, consistiu apenas em gaze embebida de plasma e gaze seca para cobrir e segurar o agregado, além de uma atadura de 13 cm envolvendo toda a parte tratada e fixada com esparadrapos. O paciente foi instruído a trocar o curativo 24 horas após o tratamento, seguindo rigorosamente essa orientação.
## III. REsultadoS E DisCussÃo
Para o desenvolvimento e aplicação da pesquisa, foi utilizado a técnica de plasma enriquecido com plaquetas (PRP) para tratar feridas de difícil cicatrização. A paciente selecionada, apresentava uma ferida aberta por cerca de 3 anos, com dimensões de dois centímetros de altura por quatro centímetros de largura no momento da anamnese e entrevista para inclusão na pesquisa. Além disso, tinha uma segunda ferida já fechada, porém com sinais de inflamação e sensibilidade local, medindo seis centímetros de largura por três centímetros de altura.As úlceras da paciente localizam-se na região do tornozelo, uma área comum para úlceras ulcerativas em pacientes com dificuldades de mobilidade, conforme protocolo do manual de feridas.
Hemograma realizado em abril de 2024 apresentava os seguintes resultados:
### Eritrograma:
- Eritrócitos: 4,19 milhões/mm3 (Referência: 3,80 a 4,80 milhões/mm3)
- Hemoglobina: 12,40 g/dL (Referência: 12,0 a 16,0 g/dL)
- Hematócrito: 36,60% (Referência: 36 a $46\%$ )
- VCM: 87,49 fL (Referência: 82 a 98 fL)
- HCM: 29,58 pg (Referência: 27 a 32 pg)
- CHCM: 33,89 g/dL (Referência: 31,5 a 34,5 g/dL)
- RDW: 13,1% (Referência: 11,6 a $14 {, } 6\%$ )
#### Leucograma:
- Leucócitos: 5.060 /mm3 (Referência: 4.000 a 10.000 /mm3)
- Eosinófilos: $0\%$ - 0,0 /mm3 (Referência: 0 a $6\%$ - 0 a 600 /mm3)
- Bastões: 0% - 0,0 /mm3 (Referência: 0 a $6\%$ - 0 a 600 /mm32)
- Segmentados: $42\%$ - 2125,2 /mm3 (Referência: 40 a $75\%$ - 2000 a 7500 /mm3)
- Linfócitos: $45\%$ - 2277,0 /mm3 (Referência: 20 a 45% - 1000 a 5000 /mm3)
- Monócitos: 10% - 506,0 /mm3 (Referência: 0 a 10% - 0 a 1000 /mm3)
#### Plaquetas:
Plaquetas: 183.000 /mm3 (Referência: 150.000 a 400.000 /mm3)
Durante a aplicação do plasma, a paciente não apresentou nenhum desconforto significativo. Ela relatou sentir após a aplicação no local, um repuxamento de pele, dolorido, avermelhado, com formigamento e uma dor constante e latejante na região da ferida.Fram seguimos os mesmos protocolos estabelecidos na primeira sessão para garantir a continuidade e consistência do tratamento (Figura 1).
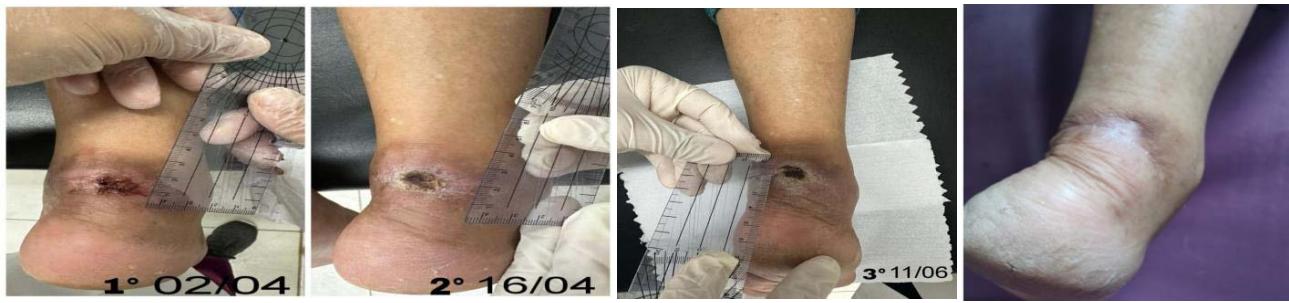
Figura 1: Evolução Da Ferida Até A Cicatrização Completa
Segundo o Manual de Padronização de Curativos (2021), ferida é qualquer lesão causada que interrompa a continuidade da pele, podendo atingir a epiderme, a derme, tecido subcutâneo e a fáscia muscular, chegando a expor estruturas profundas do organismo. As feridas são classificadas segundo diversos parâmetros, que auxiliam no diagnóstico, evolução e definição do tipo de tratamento, tais como cirúrgicas, traumáticas e ulcerativas. A ferida da paciente é traumática e ulcerativa. Traumáticas são feridas provocadas acidentalmente por agentes mecânicos, como um prego, espinho ou por pancadas; e feridas ulcerativas que são lesões escavadas, circunscritas, com profundidade variável, podendo atingir desde camadas superficiais da pele até músculos.
As feridas crônicas são aquelas que não cicatrizam espontaneamente e que requerem um período de tempo maior que 12 semanas para cicatrizar e, frequentemente, apresentam repetidamente vários processos infecciosos ou, até mesmo, quando associadas com patologias sistêmicas pode prejudicar o processo de cicatrização como por exemplo a doença Diabetes. Diante da complexidade, a cicatrização dos ferimentos é um processo dinâmico que envolve fenômenos celulares e moleculares que interagem para que ocorra o reparo tecidual.' É administrado por eventos de coagulação, inflamação, formação de tecido de granulação, epitelização e remodelamento tecidual, os quais são mediados e modulados por citocinas e fatores de crescimento (Nascimento et al., 2024).
Segundo O Manual De Avaliação E Tratamento De Feridas (2021), Existe 3 Fases Para A Cicatrização:
Fase De Inflamação Ou Exsudativa: A primeira fase de hemostasia e inflamação iniciam-se com a ruptura de vasos sanguíneos e o extravasamento de sangue. A lesão de vasos sanguíneos é seguida rapidamente pela ativação da agregação plaquetária e da cascata de coagulação, resultando na formação de moléculas insolúveis de fibrina e hemostasia. Durante este processo ocorre o recrutamento de macrófagos e neutrófilos. Ocorre reação completa do tecido conjuntivo vascularizado em resposta à agressão do tecido, o objetivo é interromper a causa inicial (dor, calor rubor e edema).
- Fase Proliferativa (Granulação E Reepitelização): Caracteriza-se pela neovascularização e proliferação de fibroblastos, com formação de tecido róseo, mole e granular na superfície da ferida. Contudo, a formação do tecido de granulação é estimulada por níveis baixos de bactérias na ferida, mas é inibida quando o nível de contaminação é elevado.
- Fase De Maturação Ou Remodelagem Do Colágeno: E a fase final de cicatrização de uma ferida que se caracteriza pela redução e pelo fortalecimento da cicatriz. Durante esta fase, os fibroblastos deixam o local da ferida, a vascularização é reduzida, a cicatriz se contrai e torna-se pálida e a cicatriz madura se forma (de 3 semanas a 1 ano a mais). O tecido cicatricial sempre vai ser menos elástico do que a pele circundante.
Pacientes diabéticos apresentam uma predisposição para desenvolver feridas crônicas, uma vez que ela envolve múltiplos sistemas, além da idade, alimentação, medicamentos, nutrição, infecções que podem comprometer a cicatrização tecidual. As feridas são consideradas um problema grave e de abrangência mundial, responsáveis por significativos índices de morbidade e mortalidade (OLIVEIRA et al., 2019).
O PRP mostrou potencial ao liberar fatores de crescimento que estimulam a regeneração tecidual e a formação de vasos sanguíneos, essenciais para a cicatrização de úlceras crônicas. A pesquisa continua sendo crucial para otimizar os protocolos de tratamento, superar as variabilidades na preparação do PRP e definir melhor suas aplicações clínicas específicas. Compreender os mecanismos moleculares e celulares envolvidos na cicatrização de feridas, especialmente em pacientes com comorbidades como diabetes, é fundamental para melhorar os resultados clínicos e a qualidade de vida desses pacientes (Nascimento_ et al., 2024).
Muito importante o desenvolvimento de terapias personalizadas que considerem as necessidades individuais dos pacientes e que promovam a cicatrização eficaz das feridas. Este estudo reforça a importância do PRP como uma alternativa viável e promissora para o tratamento de úlceras nos pés diabéticos, destacando a necessidade de mais pesquisas para validar e expandir seu uso clínico.
## IV. CONCLUSÃO
A pesquisa e aplicação do plasma rico em plaquetas (PRP) para o tratamento de feridas crônicas, especialmente em pacientes diabéticos, mostraram-se promissores, apesar dos desafios e variabilidades associadas àaplicação do PRP.Por fim, os avanços nesta área oferecem esperança real para melhorar a gestão e o tratamento de feridas crônicas, impactando positivamente a vida dos pacientes afetados.
Generating HTML Viewer...
References
9 Cites in Article
Aline Oliveira,Daniel Rocha,Sandra Bezerra,Elaine Andrade,Ana Santos,Lídya Nogueira (2019). Qualidade de vida de pessoas com feridas crônicas.
Peter Everts,Kentaro Onishi,Prathap Jayaram,José Lana,And Mautner (2020). Platelet-Rich Plasma: New Performance Understandings and Therapeutic Considerations in 2020.
S (2020). <em>Science</em>Adviser: No, NIH researchers didn’t pocket $710 million in pandemic royalties.
Shyla Gupta,Et Gupta,Al (2020). Evidence-Based Indications of Platelet-Rich Plasma Therapy. Evidence-Based Indications of Platelet-Rich Plasma Therapy.
Viktor Kunder,Al (2023). The use of Platelet-Rich Plasma in the Treatment of Diabetic Foot Ulcers: A Scoping Review. The use of Platelet-Rich Plasma in the Treatment of Diabetic Foot Ulcers: A Scoping Review.
André Dutra (null). Memórias de educadoras sobre a gestão de Paulo Freire na Secretaria Municipal de Educação de São Paulo.
Olukemi Olufemi,Adeolu Adeyeye (2017). Irrigation solutions in open fractures of the lower extremities: evaluation of isotonic saline and distilled water.
Wanderlene Nascimento,Oliveira De,Et Do,Al (2024). Utilização Do Plasma Rico Em Plaquetas E Da Fibrina Rica Em Plaquetas Na Cicatrização De Feridas Crônicas.
No ethics committee approval was required for this article type.
Data Availability
Not applicable for this article.
How to Cite This Article
Dr. Ana Elizabeth Oliveira de Araujo Alves. 2026. \u201cUse of Platelet-Rich Plasma (PRP) in the Treatment of Difficult-Healing Wounds: Case Report\u201d. Global Journal of Medical Research - K: Interdisciplinary GJMR-K Volume 25 (GJMR Volume 25 Issue K3): .
Explore published articles in an immersive Augmented Reality environment. Our platform converts research papers into interactive 3D books, allowing readers to view and interact with content using AR and VR compatible devices.
Your published article is automatically converted into a realistic 3D book. Flip through pages and read research papers in a more engaging and interactive format.
Subject: Global Journal of Medical Research - K: Interdisciplinary
Authors:
Dr. Ana Elizabeth Oliveira de Araujo Alves, Dr. Anny Kelly Rocha de Oliveira Ferreira, Dr. Bruna Lorrany Mariano Rodrigues, Dr. Dalila Estefânia Mariano Souza, Dr. Elizabete Rocha de Oliveira Gonçalves, Dr. Marina Firmino Lima de Oliveira (PhD/Dr. count: 6)
Our website is actively being updated, and changes may occur frequently. Please clear your browser cache if needed. For feedback or error reporting, please email [email protected]
Thank you for connecting with us. We will respond to you shortly.